نظریه ی کوانتومی چیست؟
نظریه کوانتومی چیست؟
هدف:
نظریه کوانتومی که با نام های فیزیک کوانتومی یا مکانیک کوانتومی نیز شناخته می شود، شاخه ای از فیزیک است که رفتار و برهم کنش ماده و انرژی را در مقیاس ذرات ریز اتمی و در دمای پایین مورد بررسی قرار می دهد. مرتبه و مقدار بزرگی این ذرات در حال بر هم کنش را با یک ثابت فیزیکی بسیار کوچک به نام ثابت پلانک مقایسه می کنند. نگران نباشید!!!
در این مطلب می خواهیم به مفاهیم مقدماتی در این نظریه مانند فوتون، ثابت پلانک، دوگانگی موج و ذره، عدم قطعیت و ... اشاره کنیم تا معانی و مفهوم این واژه های عجیب را بهتر متوجه شوید!
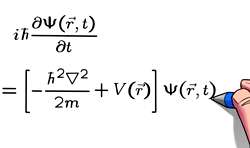
شرح درس:
فوتون چیست؟

کوچکترین ذرات تشکیل دهنده ی نور را که امکان دیدن تک تک آن ها وجود ندارد، فوتون نام دارند. اولین فوتون های این جهان احتمالا پانزده میلیارد سال پیش و در حین فرایند انفجار بزرگ (بیگ بنگ) به وجود آمده اند. بنابراین به یک ذره کوانتومی از تابش الکترومغناطیسی، فوتون می گویند.
حتما می پرسید خود کوانتوم به چه معناست؟
به کوچکترین واحد یک کمیت یا کوچکترین بخش هر چیزی، کوانتوم گفته می شود.
پس یک کوانتوم از انرژی الکترومغناطیسی را یک فوتون نام گذاری می کنند که با سرعت نور منتشر می شود.
مفهوم فوتون و کوانتوم در مکانیک کوانتومی یا نظریه کوانتومی بیان می شود. نظریه کوانتومی، یک مدل ریاضی است که برای توصیف رفتار ذراتی در مقیاس اتم و یا ریزتر از اتم به کار می رود. نظریه کوانتومی نشان می دهد که ماده و انرژی کوانتیزه هستند؛ یعنی در بسته های جداگانه ای و در ابعاد بسیار ریز در جهان به وجود می آیند.
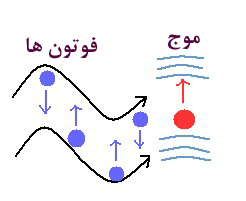
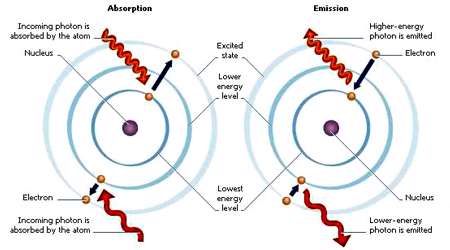
یک فوتون می تواند خواص ذره ای یک موج الکترومغناطیسی را هم نشان دهد. یعنی این که می توانیم موج الکترومغناطیسی را به صورت یک موجی که از ذره های بسیار ریزی به نام فوتون تشکیل شده است، تصور کنیم. این که موج الکترومغناطیسی هم خاصیت ذره ای دارد و هم خاصیت موجی، تصور درستی است؛ برای مثال، پدیده های پراش و تداخل را با مفهوم موجی بودن نور الکترومغناطیسی می توان بهتر فهمید و توضیح داد و پدیده هایی مانند جذب و انتشار نور را با خاصیت ذره ای موج الکترمغناطیسی می توان بهتر فهمید.
ممکن است فکر کنید فقط نور مرئی است که از بی نهایت فوتون تشکیل شده است؛ انواع دیگر امواج الکترومغناطیسی نیز از فوتون تشکیل یافته اند، یعنی طول موج های مختلف موجود در طیف الکترومغناطیسی، دارای فوتون هایی با انرژی و بسامد متفاوت هستند. به عنوان مثال، فوتون هایی که اشعه ایکس از آن ها تشکیل یافته است، با طول موج کوتاه و انرژی زیاد منتشر می شوند. برای همین است که از تماس با اشعه ایکس و فرابنفش باید اجتناب شود زیرا با وجود فوتون هایی که از این اشعه ها به سطح بدن می رسد، بیماری و سوختگی پوست حاصل می شود.
زمانی که فوتون ها به دیگراتم ها برخورد می کنند، باعث می شوند برخی الکترون های متعلق به اتم ها با سرعت بیشتری حرکت کنند؛ این همان احساس گرمایی است که با نشستن در مقابل نور خورشید به ما دست می دهد.
ثابت پلانک چیست؟
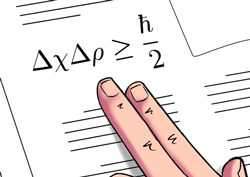
ثابت پلانک که در فیزیک کوانتومی آن را با h نشان می دهند، یک مقدار بسیار کوچک است که انرژی تابش الکترومغناطیسی یک ذره کوانتومی (مانند فوتون) را به فرکانس تابش آن مربوط می کند. در دستگاه SI، مقدار این ثابت را به طور تقریبی6.626176 x 10-34 ژول ضرب در ثانیه است.
انرژی E یک فوتون در یک موج الکترومغناطیسی به طور مستقیم به فرکانس تابش این موج مربوط می شود که معادله آن به شکل زیر است: E = hν
که ν (نو) بسامد تابش موج است و h ثایت پلانک است که انرژی را به بسامد مربوط می کند. ثابت پلانک مقدار و مقیاس دنیای ریز را به ما نشان می دهد. انرژی کل موج الکترومغناطیسی، مجموع انرژی های تک تک فوتون هایی است که در این موج وجود دارند.
دوگانگی موج و ذره:
این اصل بیان می کند که تمام مواد هم خاصیت موجی از خود نشان می دهند، هم خاصیت ذره ای. برای این که مفهوم دو گانه بودن خاصیت موجی و ذره ای را در مکانیک کوانتومی متوجه شویم، باید آزمایش هایی مانند اثر کامپتون، اثر فوتو الکتریک، طول موج دوبروی و فرمول پلانک برای تابش جسم سیاه را انجام دهیم. تمام این آزمایش ها این اصل دو گانگی را تایید می کنند.
دانشمندان بسیاری تاکنون آزمایش های برای نور انجام داده اند تا ثابت کنند نور هر دو خاصیت موجی و ذره ای را دارد. در سال 1901 ماکس پلانک آزمایشی انجام داد که موفق به مشاهده طیف نور مرئی از یک جسم نورانی شد و بعدها انیشتین بود که بیان کرد تابش الکترومغناطیسی از ذرات ریزی به نام فوتون تشکیل شده است. شرح این آزمایش ها را بعدها خواهید دانست.
عدم قطعیت:
اصل عدم قطعیت بیان می کند که دو ویژگی مخصوص فیزیکی را مانند اندازه حرکت و مکان یک ذره یا جسم، نمی توان به طور هم زمان و با دقت زیاد اندازه گیری کرد؛ یعنی اگر انداره حرکت ذره را بتوان با دقت زیاد اندازه گرفت، نمی توانیم با قاطعیت بگوییم مکان ذره دقیقا کجاست و برعکس.
به بیان دیگر اصل عدم قطعیت بیان می کند، اندازه گیری موقعیت یک ذره با دقت زیاد باعث می شود دقت اندازه گیری در مورد اندازه حرکت ذره، کم تر شود و برعکس.





افزودن دیدگاه جدید